国家药监局版药包材GMP来了药包材产业或将迎来“大考”
生产企业规范生产行为,指导MAH履行好药包材供应商审核职责,2022年6月2日,国家药监局官网发布了《药包材生产质量管理规范》(征求意见稿),征求意见截止日期为2022年7月2日。此规范被业界人士称为国家药监局版药包材GMP,药包材产业或将迎来“大考”。本文为大家梳理了药包材GMP实施关键点,可供药包材生产企业的内部或外部认证以及客户的合同目的,也可供MAH执行药包材供应商审计参考使用。
药品包装用材料、容器(以下简称“药包材”),主要是指与药品非间接接触的包装材料和容器,也包括功能性次级包装材料、表面印刷材料、组件和给药装置等,是药品必不可少的组成部分,它伴随着药品的生产、流通和使用全过程,因此药包材对于保证药品的安全性、有效性起着重要的作用,对药包材生产企业的审查和监管就显得很重要。我国药包材监督管理是一个从无到有、逐渐完备、循序渐进的过程,概括起来主要经历了四个阶段(“没有一点限制管理”阶段“药包材生产企业许可证制度”阶段“药包材的注册审批”阶段关联审评审批制度”阶段)。目前药包材生产质量监管环节的基础还比较薄弱,还有相当多的企业经营者质量意识跟不上,GMP管理人才匮乏,药包材实施备案制,关联审评后,药包材GMP管理亟待加强。我国药品监管部门慢慢地认识到药品包装对于药品的重要性,对药包材的监管也日趋科学、规范。行业协会、省局、国家局陆续制定有关政策法规,梳理如下:
1)省药监局版药包材GMP:2015年12月7日,广东省药包材生产质量管理指南,该指南推荐使用于广东省辖区内药包材生产公司制作质量管理全过程,要求药包材生产企业应制定符合药包材质量管理的质量方针和质量目标。并依照产品的特点,建立生产质量管理体系,并保持有效运行。
2)行业协会版药包材GMP:2019年5月8日,中国医药包装协会官网发布《药包材生产质量管理指南》(T/CNPPA 3005-2019)被业界人士称为行业协会版药包材GMP,
3)国家药监局版药包材GMP:2022年6月2日,国家药监局官网发布了《药包材生产质量管理规范》(征求意见稿),征求意见截止日期为2022年7月2日,此规范被业界人士称为国家药监局版药包材GMP,共14章72条,9千多字,明确本规范是药包材生产企业建立药包材质量管理体系的重要依据,是药包材生产管理和质量控制的基础要求。本规范旨在最大限度地降低药包材生产的全部过程中污染、交叉污染、混淆和差错的风险,确保持续稳定地供应符合药用要求和预定用途的药包材。
《药包材生产质量管理规范》(征求意见稿),共14章72条,9千多字,明确了药包材生产企业质量管理、机构与人员、厂房与设施、设备、物料与产品、确认与验证、文件管理、生产管理、质量控制与质量保证、委托生产与委托检验、产品发运与召回、用户管理服务等要求,既考虑结合药包材生产实际管理精准施策,又考虑落实药包材备案制度;既突出重点产品、关键环节管理,又注重实操性,保证政策落地,将逐步提升我国药包材生产质量管理的整体水平,指导和督促企业持续稳定地生产出质量安全、符合标准要求的药包材,条款详见下表:
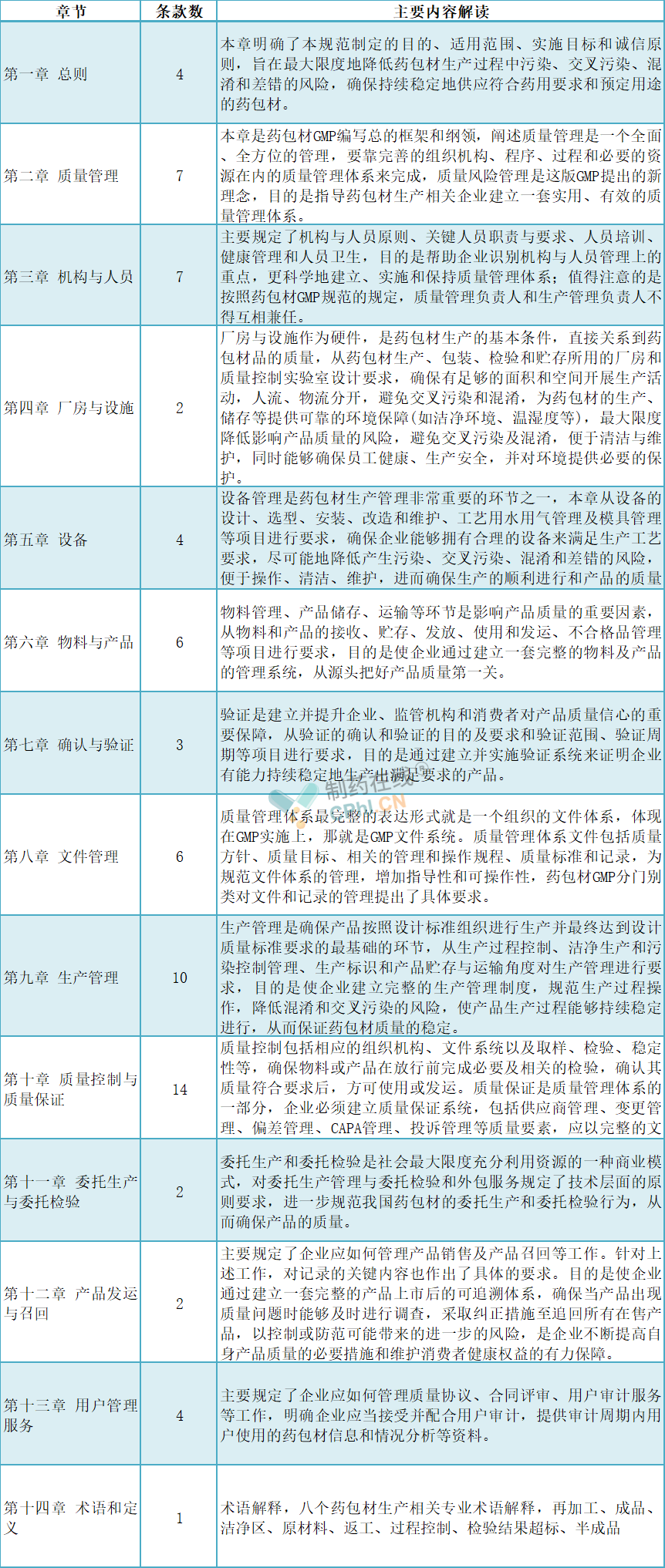
当前,我国药包材生产公司制作和质量管理上的水准差异较大,《药包材生产质量管理规范》的落地实施,必将成为2022年药包材监管制度改革的亮点,药包材产业或将迎来“大考”,成为药包材行业发展的里程碑,一定会大幅度的提高我国药包材监督管理质量,规范药包材生产和质量行为,保障药包材使用安全,促进中国药包材产业健康持续发展。


